Het EMA heeft deze mogelijkheden na een succesvolle pilot van twee jaar toegevoegd aan het begeleidingsprogramma PRIME (Priority Medicines) voor innovatieve geneesmiddelen die een belangrijke medische meerwaarde kunnen bieden. PRIME is bedoeld voor geneesmiddelen voor ernstige aandoeningen waarvoor nog weinig of geen goede behandelingen beschikbaar zijn. Het programma biedt vroege, proactieve begeleiding aan geneesmiddelontwikkelaars, waaronder intensieve wetenschappelijke advisering en een versnelde beoordeling van de handelsvergunning (150 in plaats van 210 dagen), met als doel patiënten sneller toegang te geven tot innovatieve behandelingen.
Routekaart
Het eerste onderdeel is een regulatoire routekaart met een productontwikkeltracker. Deze geeft inzicht in de voortgang van een geneesmiddel en helpt risico’s en aandachtspunten tijdig in beeld te brengen, zodat ontwikkelaars en toezichthouders gedurende het hele traject beter op elkaar afgestemd blijven.
Het tweede onderdeel is versnelde wetenschappelijke advisering, bedoeld voor specifieke en kritische vragen tijdens de ontwikkeling. Ontwikkelaars kunnen hierdoor sneller duidelijkheid krijgen over de regulatoire verwachtingen die bepalend zijn voor de verdere voortgang.
Het derde onderdeel is de submission readiness meeting: een overlegmoment ongeveer een jaar voordat een aanvraag voor markttoelating wordt ingediend. Tijdens dit gesprek beoordelen het EMA en de ontwikkelaar samen of het ontwikkelprogramma op schema ligt en of er nog aanvullende gegevens nodig zijn voor een zorgvuldige beoordeling door het Comité voor geneesmiddelen voor menselijk gebruik (CHMP).
Betekenis voor behandelaars en patiënten
Op 18 maart publiceerde het EMA het evaluatierapport van de pilot. De conclusie is dat de nieuwe werkwijze leidt tot betere begeleiding van ontwikkelaars en meer flexibiliteit in het regulatoire proces. De uitbreiding van PRIME sluit ook aan bij de voorbereidingen op de nieuwe Europese geneesmiddelenwetgeving, waarin het begeleidingsprogramma een vaste plaats krijgt.
Voor de innovatieve geneesmiddelensector onderstreept deze ontwikkeling het belang van vroege en continue afstemming met toezichthouders. Door onzekerheden eerder in het proces te adresseren, kan dit bijdragen aan een efficiëntere ontwikkeling van geneesmiddelen en uiteindelijk aan tijdige toegang voor patiënten in Europa.
Het evaluatierapport staat hier.
Lees ook:

Analyse: welke medicijnen tegen kanker mist Nederland?
Bloedkanker genezen?

EU-voorstellen dramatisch voor weesgeneesmiddelen
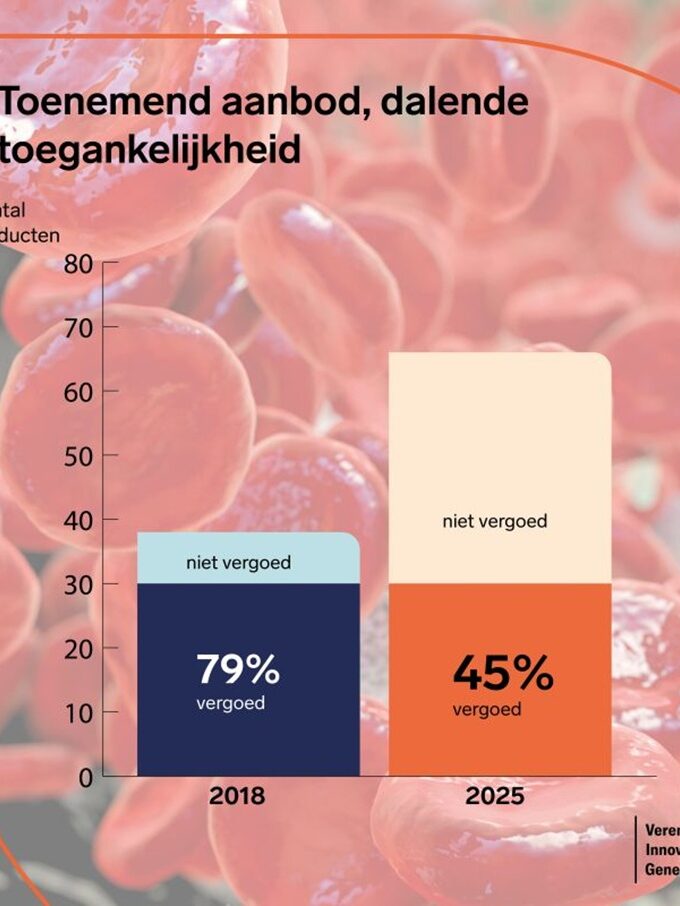
Minder dan helft van beschikbare weesgeneesmiddelen toegankelijk voor patiënten

